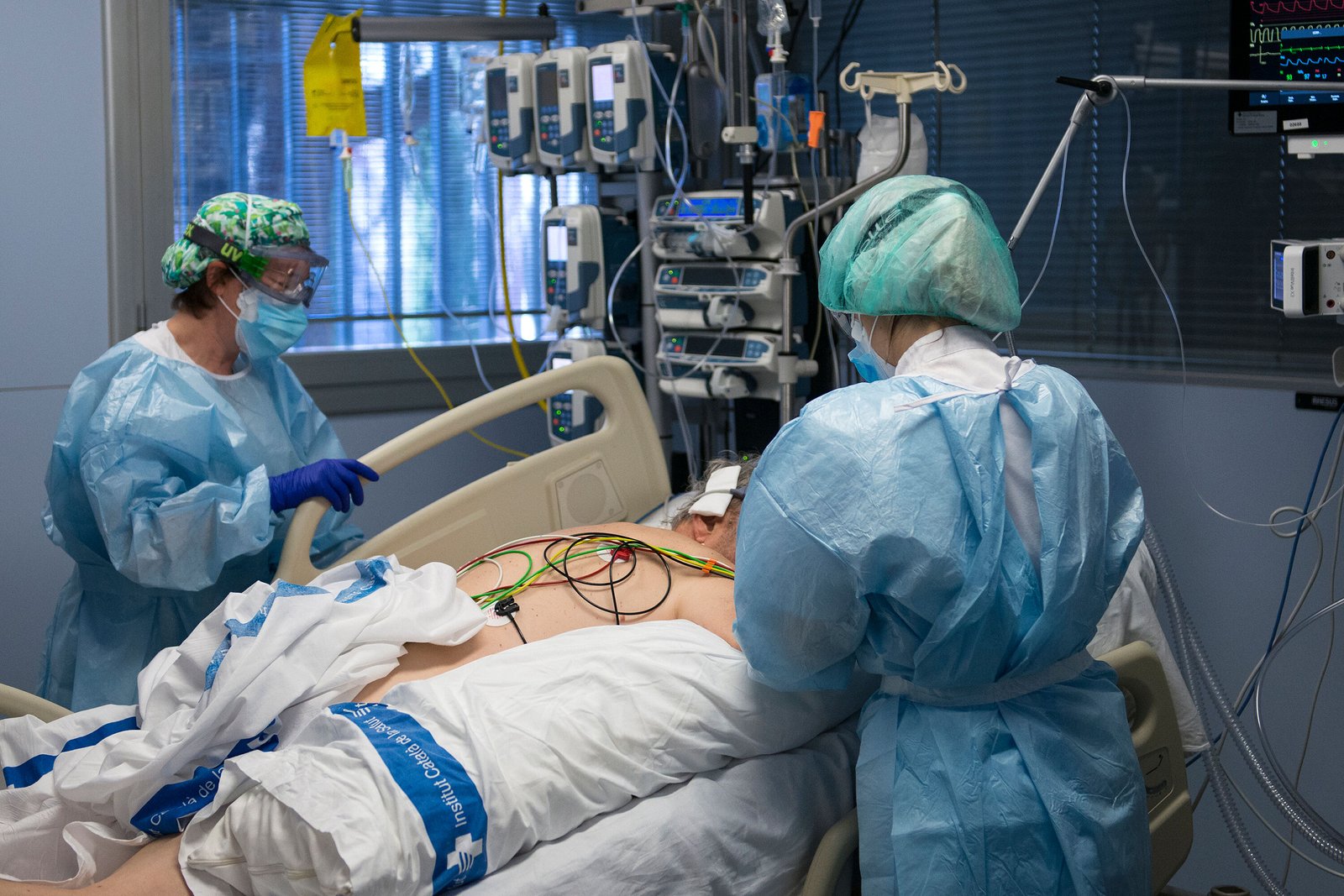
<p>En el quirófano, el paciente yacía conectado a una máquina mientras, a su lado, en una mesa auxiliar, un hígado de cerdo editado genéticamente filtraba su sangre a través de un circuito de tubos. Así, durante horas, <strong>un órgano animal asumió funciones que el hígado humano del paciente </strong>ya no podía realizar. No era un trasplante en el sentido clásico: el órgano no estaba implantado, sino trabajando desde fuera, como un puente biológico para ganar tiempo.</p>
Logran estabilizar a un paciente con insuficiencia hepática mediante un hígado de cerdo modificado genéticamente. El órgano no se trasplantó, sino que fue conectado desde el exterior
En el quirófano, el paciente yacía conectado a una máquina mientras, a su lado, en una mesa auxiliar, un hígado de cerdo editado genéticamente filtraba su sangre a través de un circuito de tubos. Así, durante horas, un órgano animal asumió funciones que el hígado humano del paciente ya no podía realizar. No era un trasplante en el sentido clásico: el órgano no estaba implantado, sino trabajando desde fuera, como un puente biológico para ganar tiempo.
Los médicos del Hospital Xijing, en la ciudad china de Xi’an, observaban en silencio los monitores. Cada hora ganada aumentaba las posibilidades de que el paciente sobreviviera lo suficiente para recibir un trasplante o para que su propio hígado empezara a recuperarse. De repente, los niveles de toxinas empezaron a descender. Los parámetros, poco a poco, mejoraban. El paciente estaba saliendo del fallo hepático.
Las televisiones estatales chinas han estado retransmitiendo esta semana algunas imágenes de un exitoso ensayo clínico que se anunció a principios de febrero y que marca un nuevo paso en la carrera por utilizar órganos de animales en humanos, una línea de investigación que China ha convertido en una de sus apuestas médicas más ambiciosas ante la escasez crónica de donantes.
«Es la primera vez que un hígado porcino mantenido extracorpóreamente logra revertir una insuficiencia hepática aguda en un paciente humano», asegura una nota de la empresa biotecnológica china ClonOrgan, que fue la encargada de editar seis genes del hígado de cerdo utilizado en el procedimiento para aumentar su compatibilidad con el tejido humano y mejorar la coagulación sanguínea.
El hígado de cerdo, explican los investigadores, se colocó en un dispositivo de perfusión y se conectó al sistema circulatorio del paciente mediante un circuito externo. Durante 66 horas, el órgano realizó funciones esenciales: desintoxicación, síntesis de proteínas y metabolismo, tareas básicas que normalmente desempeña el hígado humano.
Según el hospital, el hígado de cerdo funcionó bien, generando aproximadamente un tercio de la bilis que produce el órgano humano. Casi tres días después del procedimiento, los indicadores clave de la función hepática del paciente habían mejorado. Las últimas informaciones, del 5 de febrero, apuntaban a que los signos vitales del paciente estaban estables, con indicadores fisiológicos y bioquímicos acercándose a niveles normales.
«El sistema funciona, en la práctica, como un puente: estabiliza al paciente mientras espera un trasplante humano o mientras su propio hígado se recupera. Este enfoque reduce el rechazo inmunitario, uno de los mayores obstáculos del xenotrasplante, porque el órgano no permanece dentro del cuerpo», detalla el cirujano He Xiaoshun, uno de los especialistas más citados en este campo y director de un importante programa de trasplantes en Guangzhou.
He recuerda que el objetivo principal de estos ensayos no es todavía reemplazar completamente los órganos humanos, sino comprender cómo interactúan los órganos modificados genéticamente con el cuerpo humano en condiciones clínicas reales.
En marzo de 2024, cirujanos del Hospital Xijing ya lograron implantar el primer hígado porcino en un paciente en muerte cerebral para estudiar su funcionamiento en condiciones reales. El órgano, con seis genes editados para reducir el rechazo inmunitario y mejorar la compatibilidad con la sangre humana, permaneció activo durante diez días.
En ese tiempo, los médicos comprobaron que el hígado producía bilis, sintetizaba proteínas esenciales y mantenía funciones metabólicas básicas sin signos de rechazo hiperagudo, el principal obstáculo histórico de los xenotrasplantes. El experimento se diseñó como una prueba de viabilidad: no buscaba salvar al paciente, sino observar hasta qué punto un órgano animal podía asumir tareas fisiológicas complejas en el cuerpo durante periodos prolongados.
Ese mismo año, un equipo de la Universidad de Guangzhou realizó el primer trasplante experimental de un pulmón de cerdo en un hombre de 39 años en muerte encefálica. Durante varios días, el órgano funcionó parcialmente y permitió monitorizar su viabilidad, pero el paciente desarrolló hinchazón generalizada y acumulación de líquidos en los tejidos, probablemente por problemas de flujo sanguíneo. Aunque hubo signos de recuperación parcial, los médicos observaron pronto que el cuerpo comenzaba a rechazar el órgano.
El salto más ambicioso llegó poco después. En 2025, la revista Journal of Hepatology publicó el caso de un paciente de 71 años con cirrosis avanzada y cáncer hepático que sobrevivió casi seis meses tras recibir un hígado de cerdo modificado genéticamente en el Departamento de Cirugía Hepatobiliar de la Universidad Médica de Anhui.
Se trataba del primer xenotrasplante hepático realizado en un receptor humano vivo con seguimiento prolongado. Los médicos lograron mantener la función del injerto durante 171 días, un tiempo que, aunque no supuso una curación definitiva, demostró que un órgano animal podía sostener la vida humana durante meses.
«El uso combinado de órganos editados genéticamente y sistemas de circulación extracorpórea puede proporcionar soporte vital temporal y reducir mucho la necesidad de inmunosupresión agresiva», explica ahora Tao Kaishan, cirujano del Hospital Xijing que ha participado en el reciente ensayo. El cerdo se ha convertido en el animal preferido para este tipo de investigaciones porque sus órganos tienen un tamaño y una fisiología similares a los humanos, se reproducen rápidamente y pueden modificarse genéticamente con relativa facilidad.
La mayoría de especialistas insisten en que, por ahora, el objetivo inmediato no es reemplazar por completo los trasplantes humanos, sino ganar tiempo: días o semanas decisivas para que aparezca un donante o para que el propio órgano del paciente se recupere.
Pero Wang Lin, director de cirugía hepatobiliar del Hospital Xijing, sostiene que estas técnicas «no solo pueden dar más tiempo a los pacientes en lista de espera, sino ampliar las opciones de tratamiento para la insuficiencia hepática terminal». Según Wang, los resultados indican que los hígados porcinos podrían llegar a «sustituir o apoyar la función hepática humana» en determinados escenarios clínicos, aunque todavía queda un largo camino por recorrer.
Salud